4278 0
Показаниями к эндоскопическим операциям являются опухоли и рубцовые стенозы трахеи и крупных бронхов. Это положение нуждается в уточнениях. В первую очередь патологические изменения должны быть доступны для жесткого бронхоскопа, т. е. локализоваться в трахее, главных, промежуточном и долевых бронхах. При более глубоком расположении опухоли выполнение операции в ряде случаев возможно, но требует применения бронхофиброскопа и сопряжено с определенными техническими трудностями.
Эндоскопические операции на трахее и бронхах ни в коем случае не следует противопоставлять классическим открытым операциям, возможности и радикальность которых неизмеримо выше. Однако в связи со значительно меньшей травматичностью эндотрахеальные и эндобронхиальные операции имеют преимущества в следующих конкретных ситуациях.
Эндоскопические операции показаны при экзофитно растущих доброкачественных опухолях трахеи и крупных бронхов, когда их удаление с помощью электрокоагуляционнои петли или лазера является достаточно радикальным. Это в первую очередь относится к одиночным папилломам, при которых после технически правильно выполненного удаления обычно наступает выздоровление. Эндоскопическим способом могут быть радикально удалены довольно редко встречающиеся эндобронхиальные полипы и опухоли неэпителиального происхождения: фибромы, липомы, фибролипомы и т. д.
При множественных папилломах гортани, трахеи и крупных бронхов, склонных к рецидивам, эндоскопические операции, хотя и не являются радикальными, но могут считаться методом выбора, так как классические открытые операции, как правило, противопоказаны.
Эндоскопические операции могут быть выполнены при относительно редких экзофитно растущих и имеющих хорошо сформированную ножку так называемых типичных карциноидах трахеи и крупных бронхов. При комбинированном (в том числе интрамуральном) росте опухоли эндоскопическая операция может быть оправдана лишь в качестве первого этапа лечения при наличии осложнений или у ослабленных пациентов преклонного возраста, у которых радикальная операция представляет чрезмерный риск.
Эндоскопическая операция может быть использована в качестве паллиативного вмешательства при злокачественных опухолях трахеи и главных бронхов в следующих случаях:
- При нерезектабельных злокачественных опухолях, вызывающих нарушение проходимости трахеи и крупных бронхов с симптомами гипоксии, постстенотической инфекции, массивного кровохарканья, неукротимого кашля. В этой ситуации эндоскопическая реканализация трахеи или главного бронха с последующим введением стента позволяет вывести больного из критического состояния, устранить асфиксию и продлить жизнь больного, улучшив качество его жизни, а также дает возможность в более безопасных условиях провести курс лучевой или химиотерапии.
- При резектабельных злокачественных опухолях главных или долевых бронхов, когда тяжесть состояния больного, обусловленная выраженными вентиляционными нарушениями, постстенотической пневмонией или нагноением в обтурированных отделах легкого, не позволяет выполнить радикальную операцию. В этих случаях удаление экзофитной части опухоли, восстанавливая дренаж и вентиляцию, позволяет уменьшить интоксикацию и гипоксию, улучшить состояние больного и подготовить его к операции.
- При резектабельных злокачественных опухолях крупных бронхов у лиц преклонного возраста или больных с тяжелой соматической патологией, состояние которых делает риск радикальной операции крайне высоким, а также в случае категорического отказа больного от радикальной операции.
Показанием к эндоскопическому хирургическому вмешательству служат также грануляционные и рубцовые стенозы трахеи и главных бронхов, возникающие после трахеостомии или длительной интубации трахеи, а также (редко) после резекций и пластических операций на трахее и крупных бронхах. Эндоскопическая операция при этой патологии показана в следующих случаях:
- При наличии единичных грануляций, нередко возникающих в трахее в области трахеостомы или у конца трахеостомической канюли. При этом лазерная эвапорация может быть вполне успешной и привести к выздоровлению.
- При декомпенсированных Рубцовых стенозах трахеи, сопровождающихся выраженной дыхательной недостаточностью и/или гнойным трахеобронхитом, делающим риск радикальной операции чрезмерно высоким. В большинстве подобных случаев бронхоскопическую реканализацию трахеи выполняют в экстренном или неотложном порядке по жизненным показаниям и она является этапом подготовки больных к циркулярной резекции стенозированного участка трахеи.
- При декомпенсированных Рубцовых стенозах трахеи у больных, состояние которых требует продолжительного лечения или реабилитации и не позволяет прибегнуть к радикальному оперативному вмешательству (пациенты с неврологическими последствиями тяжелой черепно-мозговой травмы, гнойными осложнениями комбинированных травм или внутриполостных оперативных вмешательств, истощенные больные с аспирационной пневмонией при сочетании стенозов с трахеопищеводными свищами или дефектами).
- При декомпенсированных или субкомпенсированных Рубцовых стенозах трахеи большой протяженности (более 8— 9 см), наличии нескольких стенозов или участков трахеомаляции на разных уровнях трахеи, а также рецидивирующих стенозов после перенесенных ранее хирургических вмешательств на трахее, делающих ее мобилизацию и резекцию практически невозможной.
Вмешательства на грудной части трахеи и бронхах
P. KESZLER
Стремление хирурга резецировать стенозиро-ванные участки трубчатых органов с последующим восстановлением их проходимости естественно. Оперативные вмешательства с резекцией и наложением анастомозов на различных отделах пищеварительного тракта были уже широко распространены; когда только в экспериментах на животных начали проводить оперативные вмешательства на бронхах и трахее, хотя огромное значение этих операций было совершенно очевидно. Любое сужение трахеи угрожает развитием удушья, а стеноз главного бронха рано или поздно приводит к разрушению легкого. Если при этом не предоставляется возможности произвести реконструктивную операцию, остается только неизбежное удаление легкого. Реконструктивная трахеобронхиальная хирургия открывает новые перспективы, предоставляя возможности сохранения функционирующей паренхимы легкого, а при стенозе трахеи - спасая жизнь больного (Б. В. Петровский, М. И. Перельман, А. П. Кузьмичев,
1966).
Множество экспериментальных исследований, успехи
в области анестезиологии, а также разработка современных синтетических тканей и атравматики способствовали началу клинических исследований в области хирургии трахеоброн-хиального дерева. В последнее десятилетие многие хирурги получили обнадеживающие результаты. Опыт хирургии в этой области все более обогащается.
Анестезия
Необходимой предпосылкой операций на трахее н бронхах является интубационный наркоз. Этот метод позволяет достаточно широко вскрыть основную воздухоносную магистраль на подходе к патологически измененному участку. Оперативное вмешательство протекает без нарушения вен-
тиляции и газообмена, в условиях полной гарантии от аспирации крови.
При оперативных вмешательствах на долевых бронхах производится интубация трубкой с надувной манжеткой, выделяют главный бронх и отжимают его на время вмешательства мягким атравматичным зажимом. Во многих случаях применяется раздельная вентиляция легких и изоляция с помощью (двухтубусных) двухпрос-еетпых трахеальных трубок (Carlens, Gordon, Mcintosil). Эти трубки, в зависимости от того, в какую сторону они изогнуты, могут быть использованы для интубации левого или правого бронха. Трубка Kiprenski имеет узкую раздуваемую манжетку, обеспечивающую вентиляцию верхнедолевого бронха (рис. 3-96). Двухпрос-ветные трубки имеют и недостатки: они не всегда полностью соответствуют необходимым параметрам, не всегда достаточно хорошо размещаются и из-за сравнительно узкого просвета не всегда удается достаточно хорошо отсасывать мокроту и вентилировать легкие.
В тех случаях, когда оперативное вмешательство производится на шейном или верхнем грудном отделе трахеи, интубация начинается оро-трахеально. После оперативного выделения участок трахеи дистальнее сужения приподнимается; затем рассекают ее переднюю стенку и вниз вводят стерильную трахеальную трубку,
раздувают ее манжетку и соединяют с наркозным аппаратом (рис. 3-97).
Обеспечив надежную вентиляцию, производят резекцию измененной части трахеи и восстанавливают ее непрерывность. Под конец оротрахеальная трубка проводится через реконструированный участок трахеи, вторая трубка извлекается из просвета трахеи и разрез в ее передней стенке зашивается узловыми швами. В тех случаях, когда трахея вскрывается над бифуркацией бронхов, вентиляция легких осуществляется трансбронхиальным путем.
На уровне отхождения правого главного бронха разрезают его переднюю стенку и через разрез вводят в

Рис.
3-96. Интубационная трубка с двумя просветами и узкой бронхиальной манжеткой обеспечивает возможность вмешательства с обеих сторон на открытых бронхах. а)
Интубация справа, операция слева, б)
интубация слева, операция справа
левый главный бронх трубку с раздуваемой манжеткой. При такого рода интубации обеспечивается вентиляция в левом легком (рис. 3-У8а).
Более сложным является положение, когда возникает необходимость резецировать всю бифуркацию и следует достаточно широко раскрыть трахею и оба главных бронха. Представляется возможность трансторакально достаточно надежно интубировать один из главных бронхов или одновременно оба главных бронха стерильными ца-нюлями (рис. 3-986).
Такого рода интубация может применяться лишь при отсутствии возможности применения лучшей методики. Совершенно очевидно, что обе введенные в бронхи трубки мешают выполнить существенную часть опера-
рис.
3-97. Двухэтапная интубация для операции при стенозе трахеи. Дистальнее стеноза просвет трахеи вскрывается и интубируется стерильной трубкой
Рис.
3-98. Трансбронхиальный наркоз для обеспечения операций на торакальной части трахеи, а)
Интубация левого главного бронха из правого главного бронха, б)
интубация обоих главных бронхов
ции. Их трудно расположить так, чтобы они не сместились во время операции и не перекрывали бы просвета верхнедолевых бронхов, нарушая при этом их вентиляцию. В связи с этим все больше сторонников проведения этих операций при обеспечении экстракорпорального кровообращения
путем феморо-феморального bypass-шунта (Woods Nissen, Adkins,
1961, 1964). Преимущества этого метода состоят в том, что отпадает необходимость в мешающих оперировать интубационных трубках, газообмен становится оптимальным.
Оперативный доступ
Шейный отдел трахеи находится поверхностно, грудная же часть ее отклоняется от продольной оси тела дорзально под углом в 20-25°. Позади рукоятки грудины трахея еще довольно доступна, дистальнее же, углубляясь, она проходит уже позади крупных сосудистых магистралей. Бифуркация трахеи и главные бронхи покрыты задним листком перикарда. В связи с этим медиальная стернотомия позволяет получить достаточно обширный доступ только в пределах верхней апертуры грудной клетки. Грудную часть трахеи можно наиболее широко обнажить через правосторонний стандартный торакотомический доступ. Грудная клетка вскрывается в IV или V межреберном пространстве. После пересечения непарной вены открывается доступ к бифуркации трахеи. При этом становится возможным вывести в рану оба главных бронха.
При некоторых операциях, в связи с широким распространением патологического процесса по грудной части трахеи в интересах радикальности реконструктивного оперативного вмешательства необходимо получить доступ и к шейному отделу трахеи. Qrillo (1963) предложил для этого комбинированный доступ. Больного оперируют в положении лежа на спине. Проводится шейно-медиастинальный разрез, срединная стернотомия. Из этого разреза после перевязки внутренних грудных артерии и вены в IV или V межреберном пространстве поперечным разрезом широко раскрывается правая плевральная полость. При этом нет необходимости проводить стернотомию на протяжении всей грудины; вполне достаточно рассечь грудину только до межреберного пространства, избранного для поперечной торакото-мии, чтобы затем повернуть разрез вправо. Таким разрезом достигается весьма широкий доступ ко всей трахее, ее бифуркации и правому легкому.
Из левостороннего торакотомического доступа можно оперировать только на главном бронхе левого легкого. В тех случаях, когда возникает необходимость в т. н. высокой реконструкции левого главного бронха (т. е. во вмешательстве непосредственно под бифуркацией), на необходимом отрезке производят широкую мобилизацию нисходящей части аорты. Для этой цели выделяют, перевязывают и пересекают межре-
берные артерии трех межреберных пространств, несколько отступя от их выхода из аорты. Выделенный участок нисходящей части аорты берется на держалки и отводится в вентральном направлении.
Пластика трахеи и бронхов
Бронхотомия (разрез бронха) производится, если необходимо удалить из просвета бронха инородное тело или обследовать его внутреннюю поверхность. В целях бронхотомии переднюю стенку бронха, участок наибольшей выпуклости прошивают двумя, располагающимися рядом нитями, наложенными П-образно вокруг близлежащих хрящей бронха («держалки»). Между «держалками» поперечно рассекается передняя стенка бронха. При потягивании за «держалки» просвет бронха достаточно широко растягивается, и его можно рассмотреть при помощи изгибаемого осветительного шпателя. После окончания необходимой процедуры разрез бронха зашивается узловыми швами (рис. 3-99). Швы не должны вызвать стенозирование или изгиб бронха. Если обследуемый бронх небольшого калибра или предполагается иссечение с образованием дефекта стенки бронха, то нельзя ограничиться простым ушиванием разреза, так как это может привести к сужению бронха. Отверстие должно быть закрыто, как в случаях закрытия окончатого дефекта после эксцизии опухоли или стенози-рованного участка.
Закрытие окончатого дефекта.
Для закрытия окончатых дефектов применяются собственные и консервированные ткани. Сравнительно небольшой дефект диаметром не более 1 см
можно закрыть путем свободной пересадки лоскута из пери-

ряс.
3-99.
Бронхотомия а)
поперечным разрезом между двумя хрящевыми кольцами, б)
закрытие разреза бронха узловыми швами

Рис. 3-100. Закрытие дефекта стенки трахеи после правосторонней пневмонэктомии в случае перехода опухоли на стенку трахеи а)
после иссечения латеральной части стенки трахеи; б)
для закрытия дефекта используется часть медиальной стенки
карда или широкой фасции бедра,
можно применить консервированную широкую фасцию бедра или консервированный лоскут из твердой мозговой оболочки. Если дефект стенки возник при оперативном вмешательстве по поводу тра-хеального или бронхо-пищеводного свища, или трахеальной кисты, то в этих случаях для закрытия свищевого отверстия или отверстия кисты можно использовать стенки тканей свищевого хода или кисты.

Рис. 3-101.
Закрытие дефекта стенки левого главного бронха после резекции верхней доли в случае перехода опухоли на стенку главного бронха, а)
Резекция латеральной части стенки главного бронха; б)
для закрытия дефекта используется часть стенки язычкового бронха
В том случае, когда карцинома (или аденома) правого бронха распространилась на боковую стенку трахеи и производится удаление правого легкого, обработку главного бронха этого легкого нельзя производить по общепринятой методике. Эти опухоли удаляются из трахеи вместе с инфильтрированным участком ее стенки в пределах видимых здоровых тканей; проводится экстренное гистологическое исследование (А. И. Пирогов,
1975). При этом щадится медиальная стенка главного бронха. Из этой стенки образуют лоскут
на ножке,
которым прикрывается образовавшийся дефект. Лоскут подшивается по краям (Neville,
1965) (рис. 3-100).
По этому принципу могут производиться и другие пластические операции в различных частях бронхиального дерева. Этот принцип применим в тех случаях, когда, например, доброкачественная опухоль исходит из левого главного бронха и переходит на верхнедолевой бронх. При этом рассекается главный бронх, иссекается его измененная часть, производится резекция верхнедолевого бронха. Верхнедолевой бронх отсекается так, чтобы из язычкового бронха можно было выкроить лоскут на ножке, поместить его на овальный дефект, образовавшийся после резекции стенки главного бронха, и, повернув, вшить там (рис. 3-101).
Для закрытия больших окончатых дефектов трахеи наиболее выгодно использовать лоскуты на ножке из мышцы и надкостницы межреберно-реберного пространства.
Для этого на протяжении кожного разреза резецируют IV или V ребро и в вентральном углу этого разреза формируют необходимой величины лоскут из межреберной мышцы вместе с надкостницей. Таким путем можно без особых трудностей выделить в
Рис. 3-102. Закрытие дефекта стенки трахеи межреберным мышечно-надкостничным лоскутом на ножке
центральном направлении хорошо кровоснаб-жаемый мышечно-надкостничный лоскут шириной 2-2,5 см
и наложить его на окончатый дефект трахеи. Лоскут фиксируют узловыми швами, близко располагающимися Друг от друга по краям дефекта. Листок надкостницы располагают в сторону просвета дефекта (Blair,
1958; Narodick,
1964) (рис. 3-102).
При стенозе бронхов и трахеи предпочитают производить циркулярную резекцию и накладывать анастомоз. Однако в исключительных случаях все же еще применяют классические способы хирургии бронхов. Для этого суженный участок продольно иссекается; растягивая края разреза, устраняют стеноз. Теперь возникает необходимость пластически закрыть образовавшийся значительный овальный дефект. Для стабильного прикрытия иссеченного участка используют свободную пересадку кожного лоскута, укрепленного стальной проволокой (Oebuuer, 1950). Кожный лоскут, взятый со спины или бедра, освобождают от подкожной клетчатки, растягивают на деревянной дощечке, закрепляя по углам швами. Затем этот лоскут укрепляется стальной сеткой. При этом следует обращать внимание на то, чтобы проволока на обращенной в просвет части не выступала, а была полностью прикрыта кожей.
Анастомозы трахеи и бронхов
Стенозы или окклюзии участков воздухонос-ных путей наиболее целесообразно оперировать, производя циркулярную резекцию с последующим восстановлением непрерывности анастомоза по типу «конец в конец» (Allison, 1959). Преимуществами такого рода операции является то, что отрезки можно хорошо сшивать без натяжения, просвет воздухоносной трубки, благодаря хорошему формированию анастомоза, становится полностью проходимым.
Дискутируется вопрос о том, какой длины может быть резецируемый участок воздухоносной трубки, чтобы не было сильного натяжения на линии швов анастомоза и они бы надежно держали. Ширина хрящевых колец широко варьирует в своих размерах, как и размеры трахеи и бронхов. В общем считают возможным удалить 5-7 хрящей (3 - 4 см). Это без особого труда достигается после резекции на трахее и ее достаточной мобилизации, облегчающей наложение анастомоза между двумя разъединенными концами.
Широкая резекция производится из комбинированного стерно-торакотомического доступа. Широко выделяется и мобилизуется трахея и ее бифуркация. Вплоть до нижней легочной вены рассекается легочная связка,
выделяется все правое легкое. Это позволяет подтянуть кверху правый главный бронх примерно на 2 -3 см (Orillo,
1963). Циркулярная резекция одной из частей бронха производится, как правило, в сочетании
с резекцией соответствующей доли легкого. Доли легкого обычно настолько легко смещаются, что анастомоз после резекции бронха можно накладывать без всякого натяжения.
Более мелкие (чем долевые) бронхи обычно не подходят для наложения анастомоза. Исключением является ба-зальный бронхиальный ствол. В тех случаях, когда бронх большего диаметра должен быть соединен с просветом бронха меньшего диаметра, в целях устранения несоответствия в размерах бронх меньшего диаметра пересекается в косом направлении или производится клиновидное иссечение из его края.
Анастомозированные концы пересеченной воздухоносной трубки сводят, подтягивая за держалки, что обеспечивает наложение швов. При наложении швов необходимо следить, чтобы мембранозная часть отрезка строго соответствовала мембранозной части другого. Матрацные швы в настоящее время больше не применяются, так как они сужают просвет. Анастомоз формируют, накладывая обычный ряд узловых швов, все нити завязывают снаружи. Наиболее подходящим оказался материал, не обладающий гигроскопическими качествами: полиамид, мерсилен, тонкая стальная проволока и резорбируемый хром-кетгут. Иглы применяются только атрав-матичные. Шов анастомоза начинают по середине задней стенки и продолжают накладывать стежки один возле другого в обе стороны с равномерными интервалами. Когда остается только закрыть переднюю стенку, накладывают оставшиеся швы, но не завязывают их, чтобы лучше проследить за надежностью накладываемых швов. После прошивания наложенные швы завязываются (рис. 3-103-3-106).
В целях предупреждения возможности возникновения циркулярного рубцового сужения линии швов можно сшивать края анастомоза так, как это изображено на рис. 3-107.
Анастомоз проверяют на герметичность при помощи контрольного повышения давления воздуха внутри воздухоносной трубки и покрытия линии анастомоза жидкостью.
Если возникнет необходимость, накладываются дополнительные швы, обеспечивающие герметичнось. Линия швов должна быть прикрыта близлежащими тканями. Это особенно необходимо
в тех случаях, когда анастомоз расположен в непосредственной близости к крупным магистральным сосудам. Так, например, следует помнить, что слева анастомоз главного бронха непосредственно прилежит к легочной артерии. В случае, если возникнет нагноение по линии швов анастомоза, может возникнуть аррозия этого сосуда. Для прикрытия линии анастомоза применяют легкое, лоскут плевры, перикард, межреберный мышечный лоскут на ножке, собственную или консервированную широкую связку бедра или твердую мозговую оболочку, которые несколькими швами фиксируют к перибронхиальным тканям или соединяют их биологическим клеем.


Рис. 3-103. Наложение трахеального (бронхиального) анастомоза, 1. а)
Оба отрезка сближаются двумя «держалками» и первый шов накладывается посередине; б)
для устранения разницы величины просвета из меньшего просвета иссекается небольшой клин
Рис. 3-104.
Наложение трахеального (бронхиального) анастомоза, II. Ряд швов задней стенки, узлы завязаны снаружи
Рис. 3-105. Наложение трахеального (бронхиального) анастомоза. III. Шов передней стенки
Рис. 3-106.
Наложение трахеального (бронхиального) анастомоза, IV. Законченный анастомоз
Рис. 3-107.
Наложение трахеального (бронхиального) анастомоза, V. Для избежания циркулярного рубцевого сужения формируют разрез мембранозной части таким образом, как это показано на рисунке
Резекцию бифуркации трахеи
производят из правосторонней стандартной торакотомии. Полная реконструкция предусматривает наложение двух анастомозов, что существенно увеличивает риск, связанный с операцией. В зависимости от дефекта, имеются различные возможности для реконструктивного вмешательства.
Обращенные друг к другу края просвета обоих главных бронхов клиновидно иссекаются и по краям образовавшихся клиньев сшиваются друг с другом так, чтобы образовался один общий просвет, соответствующий диаметру трахеи. Затем накладывается второй типичный анастомоз по способу «конец в конец» с отрезком трахеи. Этот анастомоз получил названние анастомоз-штанишки (Mathey,
1966) (рис. 3-108а).
Швы могут быть наложены достаточно надежно только при обеспечении экстракорпорального кровообращения, так как интубация бронхов мешает хорошему наложению анастомоза. Это вмешательство можно несколько упростить. Рассекается легочная связка, и ставший подвижным правый главный бронх подтягивается кверху
до трахеи, куда он и вшивается. Затем, примерно на уровне


Рис. 3-108. Резекция бифуркации трахеи. Реконструкция. а)
Анастомоз-гштанишки»; б)
правый главный бронх вшивают в трахею, левый главный бронх вшивают в межуточный бронх
устья верхнедолевого бронха, накладывают круглое отверстие на межуточный бронх, в которое по способу «конец в бок» вшивают анастомоз левого главного бронха (Barclay,
1957; рис. 3-1086).
Такого рода вмешательство можно провести и с обычной интубацией бронхов. М. И. Пе-рельман
(1972) предложил методику, снижающую опасность возникновения недостаточности швов, однако при этом жертвуют частью дыхательной поверхности. При таком методе после наложения анастомоза между трахеей и главным бронхом правого легкого полностью ушивается просвет левого главного бронха. Как показал опыт многолетних наблюдений, возникающий ателектаз левого легкого, кроме потери дыхательной поверхности, особых изменений не вызывает.
Замещение больших дефектов трахеи
Замещение больших дефектов трахеи и по сей день является неразрешенной проблемой, несмотря на то, что все увеличивается число сообщений об успешных операциях. Протезы трахеи
соответствуют своему назначению, если обеспечивают замещение воздухоносной трубки на достаточно длительный срок. Кроме того, протез должен легко сшиваться с тканями трахеи, обладать тканевой совместимостью и покрываться по краям прорастающим эпителием.
Первое успешное применение протеза трахеи осуществил Gebauer (1950). Он применил аутоал-лопластический кожный лоскут на каркасе из стальной проедлоки. По его методу, из кожи спины или бедра больного заготавливается кож-ный лоскут, соответствующий дефекту трахеи. Этот лоскут освобождают от жировой клетчатки и заводят в него спираль из стальной проволоки. Сшивая друг с другом края четырехугольного лоскута, формируют протез цилиндрической формы и затем вшивают его отрезками пересеченной трахеи.
После многочисленных экспериментов на животных, когда были испробованы различные полиэтиленовые трубки, была установлена полная непригодность их для человека. На сегодня остается в силе принцип применения аутоаллоплас-тических тканей на металлической сетке или полужёстких искусственных сеток (тантал, мар-лекс, дакрон, тефлон). Сетку из такого искусственного волокна на несколько недель помещают в брюшную стенку. За этот период сетка прорастает соединительной тканью, заполняющей ее поры. Из образованной таким образом пластинки изготовляют трубку, которой замещают дефект трахеи (Beall, 1962). Если заживление в этом случае не нарушается несостоятельностью швов, то эпителий свободно прорастает со стороны трахеи на поверхность трубки, протез формируется надежно. Эпителизация протеза протекает быстрее в тех случаях, когда сохраняют у^кий перешеек мембранозной части трахеи. Такой перешеек не только служит базой эпителизации, благодаря ему предотвращается диастаз пересеченных концов трахеи (Carlens, Pearson, 1967).
Показания к операции Разрыв бронха и посттравматический стеноз
Симптомы разрыва бронха
описаны на стр. 79. Если подозрение на разрыв бронха подтверждено бронхоскопически, необходимо произвести торакотомию. Медиастинальная плевра такого больного вследствие проникновения воздуха отклонена или даже надорвана. Вокруг поврежденного места плевра покрыта интенсивным грязно-серым налетом фибрина. Вследствие аспирации определенных количеств крови легкое при пальпации плотное на ошупь. При разрыве бронха происходит расхождение его концов. Эти разошедшиеся в разные стороны концы поврежденного бронха надо обнаружить. Их измененные края иссекаются («освежаются^).
Мобилизация разошедшихся краев производится только на
таком протяжении, чтобы можно было легко наложить анастомоз. В дистальную культю бронха заводят катетер и отсасывают из легкого аспири-рованную кровянистую мокроту, после чего восстанавливают непрерывность бронха наложением анастомоза по способу «конец в конец».
Анастомоз необходимо тщательно покрыть окружающими тканями.
Если повреждение бронха своевременно не диагностировано и больной, перенеся это повреждение, благополучно поправился, то на месте повреждения бронха возникает рубцовый стеноз и вторичный ателектаз легкого. Ателектазирован-ное легкое длительное время функционирует. Поэтому даже спустя несколько лет имеет смысл резецировать стенозированный участок бронха и наложить анастомоз.
Рубцовый стеноз трахеи
Наиболее частой причиной рубцового стеноза трахеи является длительная трахеостома или интубация трахеи, также продолжающаяся длительное время. Для наиболее полноценного устранения стеноза применяется резекция суженного участка дыхательной трубки и восстанавливается ее проходимость с наложением анастомоза способом «конец в конец». Протезирование трахеи применяется только в тех случаях, когда стенозированный участок по своей протяженности настолько велик, что не представляется возможным после резекции наложить анастомоз «конец в"конец», консервативное лечение (бужирование) является безуспешным. Прежде чем решиться на широкую резекцию трахеи из шейно-торакального доступа, можно попробовать наложите Т-образный эндопротез из синтетической ткани. Введение такого протеза возможно из шейного доступа или через расширенное до необходимой степени трахеостомическое отверстие. Эндопротез выбирают в соответствии с индивидуальными размерами трахеи больного. Дистальный конец хорошо подогнанного протеза трахеи проходит ниже стенозированного участка. Горизонтальный его отрезок предохраняет от соскальзывания и позволяет отсасывать мокроту. К тому времени, когда больной привыкает к ношению протеза трахеи и приспосабливается производить откаш-ливание чер.ез эту трубку, горизонтальная часть Т-образной трубки укорачивается, края над ней зарастают. Когда через год после его введения в трахею протез извлекается, просвет трахеи становится достаточно широким. Однако бывают случаи, когда позднее вновь наступает рубцовый стеноз.
Постгуберкулезный стеноз бронха
Посттуберкулезный стеноз бронха является следствием язвенной формы туберкулеза бронха
или воспалительного процесса в лимфатических узлах.
Чаще всего дистальнее места стеноза оронха погибает соответствующая часть легкого, которую следует удалить. Сравнительно редко имеют место стенозы бронха туберкулезной этиологии, дистальнее места которых нет необратимых изменений. Если воспалительный процесс в лимфатических узлах отмечается в области правого главного бронха, верхнего долевого бронха или межуточного бронха (наиболее частая локализация), то главный или межуточный бронх может стенозироваться. Изолированное сдавливание среднедолевого бронха лимфатическими узлами было описано как среднедолевой синдром С. Л. Ли-бовым
(1955). Когда стенозирован верхнедолевой бронх и верхняя доля легкого безвозвратно разрушена гнойно-ателектатическим процессом, производят лобэктомию. При этом стремятся по возможности сохранить нижнюю и среднюю доли. Для этой цели суженный участок главного и межуточного бронхов резецируют и накладывают анастомоз. Примерно такая же ситуация (однако значительно реже) может сложиться и в отношении бронхиального дерева левого легкого.
Опухоли трахеи и бронхов
Некоторые из доброкачественных опухолей воздухоносной трубки удаляют бронхоскопически (иссечение, коагуляция). При рецидиве опухолей производят оперативное вмешательство. Характер операции зависит от размеров опухоли и ее гистологического строения. Небольшие опухоли резецируют вместе с инфильтративно измененной стенкой воздухоносной трубки, а окончатый дефект закрывают пластическим путем (см. стр. 146). При больших и злокачественных опухолях производят циркулярную резекцию воздухоносной трубки, затем восстанавливают непрерывность ее наложением прямого анастомоза. Протез из синтетического волокна может быть применен только в исключительных случаях.
Оперативные вмешательства также значительно чаще производятся на бронхах, чем на трахее. Аденома обычно исходит из главного или из долевого бронха. Поэтому сохранение дыхательной поверхности легкого после резекции бронха может быть достигнуто только пластическим восстановлением его проходимости.
Пластика бронха стала распространенным оперативным вмешательством с тех пор, как ее рациональное применение было признано в хурургии бронхиальной карциномы (Раи . В качестве методов обеспечения газообмена при операциях на трахее и ее бифуркации используют также искусственное кровообращение, гипербарическую оксигенацию, гипотермию, инжекционную вентиляцию. Для профилактики нарушений газообмена в связи с длительным выключением одного легкого прибегают к периодической вентиляции его через вторую трубку, введенную в пересеченный бронх. ИВЛ проводят в режиме гипервентиляции, параллельно корригируют сдвиги КЩС.
При операциях на легких, трахее и бронхах важно сохранять проходимость трахеобронхиального дерева (постоянная или периодическая аспирация содержимого через интубационную трубку, проверка герметичности швов), умеренно и постепенно повышать давление на вдохе до 20 - 30 мм вод. ст., тщательно расправлять оставшиеся отделы легочной ткани, создавать отрицательное давление в плевральной полости перед зашиванием грудной стенки.
Бронхоскопические оперативные вмешательства - это настоящие хирургические операции, чреватые осложнениями и неблагоприятными последствиями.
Кровотечение в просвет дыхательных путей - одно из наиболее реальных и опасных осложнений. Кровотечение чаще возникает при удалении сильно васкуляризованных доброкачественных и злокачественных опухолей трахеи и бронхов.
Причиной, как правило, бывает механическое повреждение сосудов опухоли тубусом бронхоскопа или инструментом. Но и при использовании электрокоагуляционной петли и лазерного излучения недостаточная коагуляция сосудов может осложниться кровотечением. Наиболее опасно кровотечение при выполнении операции под местной анестезией с применением бронхофиброскопа или видеоскопа. Кровь мгновенно закрывает объектив, и видимость полностью исчезает, а через узкий инструментальный канал невозможно удалить интенсивно изливающуюся кровь и образующиеся сгустки. Больной при этом может быстро потерять сознание и задохнуться, «утонув» в собственной крови. Это обстоятельство заставляет большинство бронхологов критически относиться к местной анестезии и гибким эндоскопам при выполнении эндоскопических вмешательств на бронхах и применять их лишь в редких случаях, по очень узким показаниям и при наличии веских противопоказаний к общему обезболиванию. Но и при выполнении бронхоскопической операции под общей анестезией начавшееся кровотечение даже средней интенсивности значительно затрудняет продолжение вмешательства, ухудшая видимость и делая практически невозможным использование лазера. Профилактикой кровотечения является тщательная коагуляция поверхности опухоли или области стеноза перед началом резекции.
К сожалению, заранее предсказать риск развития кровотечения можно далеко не во всех случаях, поэтому к нему нужно быть готовым всегда: иметь мощный электроотсос, запас тупферов для прижатия места кровотечения, ленту из гемостатической марли для тампонирования бронха, гемостатические растворы (е-аминокапроновая кислота, трансамча, дицинон).
При состоявшемся кровотечении , с которым удалось справиться, не следует забывать о важности тщательной аспирации из мелких бронхов, излившейся в них крови, для чего перед экстубацией необходимо выполнить санационную бронхо-фиброскопию и промывание бронхов.
Перфорация стенки трахеи или бронха.
Возникновение этого осложнения наиболее реально во время лазерной реканализации трахеи при ее рубцовом или опухолевом стенозе, а также при эвапорации опухоли с преимущественно эндофитным ростом, не имеющей четких границ. Стенку трахеи или бронха можно прожечь , если отклониться от оси просвета дыхательной трубки и углубиться в ткань рубца или опухоли в неверном направлении. Наиболее опасна перфорация стенки в тех зонах, где непосредственно к трахее или бронху примыкает пищевод или крупный кровеносный сосуд. Сквозное ранение в этом месте может осложниться развитием трахеопищеводного свища или фатальным кровотечением. Поэтому не рекомендуется производить глубокую эвапорацию опухолевой ткани в области мембранозной стенки трахеи или крупного бронха или захватывать в коагуляционную петлю мембранозную стенку трахеи при удалении исходящей из нее опухоль». Нужно быть также предельно внимательным при лазерной резекции опухолей, растущих из латеральной стенки левого главного бронха или расположенных в области шпоры правого главного бронха.
Неукоснительное соблюдение основных правил применения лазерной или электрохирургической техники является залогом безопасного выполнения эндоскопических операций.
Повредить мембранозную стенку трахеи или главного бронха можно и при попытке бужирования рубцового стеноза тубусом жесткого бронхоскопа без предварительного рассечения его лазером, так как именно мембранозная стенка трахеи является ее самым слабым местом. Даже небольшой разрыв стенки крупного бронха может осложниться развитием медиастинальной эмфиземы или пневмоторакса, нередко напряженного.
Этому способствуют инжекционная ИВЛ и кашель во время пробуждения больного и в послеоперационном периоде. Как правило, при этом в области шеи и передней грудной стенки возникает подкожная эмфизема, выявляемая по характерной крепитации.
Сквозные ранения трахеи и пищевода , а также повреждения стенок дыхательных путей, сопровождающиеся нарастающей эмфиземой средостения, требуют экстренной торакотомии и ушивания дефекта. Наряду с этим ограниченные дефекты стенки трахеи без повреждения пищевода могут зажить самостоятельно, если на время закрыть их эндотрахеальным стентом и назначить большие дозы антибиотиков, в чем мы неоднократно имели возможность убедиться.
Воспламенение световода в просвете дыхательных путей может иметь очень тяжелые последствия. Это может произойти, если использовать световоды без воздушного или газового охлаждения.
Во время бронхоскопии под общим обезболиванием с ИВЛ в просвете трахеи и бронхов создается повышенная концентрация кислорода. В насыщенной кислородом атмосфере синтетическая оболочка световода может воспламениться, что обусловливает тяжелый ожог слизистой оболочки дыхательных путей. Это также может случиться, если луч лазера попадет на введенный в трахею предмет, изготовленный из горючего материала: интубационную трубку, трахеотомическую канюлю, эндотрахеальный стент, катетер для инжекционной ИВЛ, инородное тело органического происхождения.
Приводим наблюдение.
Больной Г., 26 лет, житель Северной Осетии, во время застолья поперхнулся куском мяса и стал задыхаться. Кто-то из друзей попытался протолкнуть застрявший в гортаноглотке кусок в пищевод с помощью первой попавшейся под руку деревянной щепки. Больному удалось проглотить мясо, однако после этого у него возник постоянный кашель, а через 2 нед присоединилось стридорозное дыхание.
При ларингоскопии в подскладочном пространстве обнаружены утолщение стенки и сужение просвета трахеи, в связи с чем больной был направлен во Всероссийский онкологический научный центр (ВОНЦ) им. Н. Н. Блохина РАМН. Патология была расценена как опухоль трахеи, и было решено выполнить ее лазерную резекцию. Во время эвапорации «опухоли», производимой под общим обезболиванием с ИВЛ кислородом, произошло воспламенение фрагмента деревянной щепки, вонзившейся в стенку трахеи непосредственно под связками и вызвавшей выраженную пролиферативную реакцию, принятую за опухоль. Последовал тяжелый ожог слизистой оболочки трахеи, вызвавший развитие нескольких рубцовых стенозов на протяжении всей трахеи, наиболее значительный из которых, протяженностью около 5 см, локализовался в нижней половине грудной части трахеи.
Для дальнейшего лечения в ноябре 1997 г. больной переведен в нашу клинику с выраженным стридорозным дыханием и дыхательной недостаточностью. Выполнена лазерная реканализация трахеи, в области нижней стриктуры установлен эндотрахеальный стент Дюмона длиной 6 см, после чего больной в удовлетворительном состоянии был выписан. Циркулярная трахеальная резекция была расценена как невыполнимая в связи со множественным характером стриктур и обширностью поражения трахеи. В последующие 3 года больной был трижды госпитализирован для замены эндопротеза и удаления грануляций (рис. 1). Протяженность стенозов с каждым разом увеличивалась. Обсуждалась возможность установления бифуркационного динамического стента Фрайтага. В сентябре 2000 г. в связи с очередным ухудшением дыхания и экспекторации больной намеревался приехать в клинику, однако в начале октября у него внезапно развился приступ удушья, приведший к смерти.
Профилактикой подобных осложнений является обязательное охлаждение конца световода воздухом или сжатым инертным газом. Мы используем для этого обычный компрессор, а в последние годы - углекислый газ, баллон с которым установлен в кабинете бронхоскопии. Газ под давлением 1 - 1,5 нагнетается в пластиковый чехол световода у его проксимального конца. Благодаря этому, выполнив большое число лазерных операций в условиях общего обезболивания с инжекционной ИВЛ кислородом, мы избежали воспламенения световода в просвете дыхательных путей. Единственный случай произошел при апробации гольмиевого ИАГ-лазера, световоды которого не были оборудованы системой газового охлаждения. Поэтому, как показывает наш опыт, при адекватной продувке оболочки световода опасность ее воспламенения невелика даже при выполнении операции под общим обезболиванием с ИВЛ.
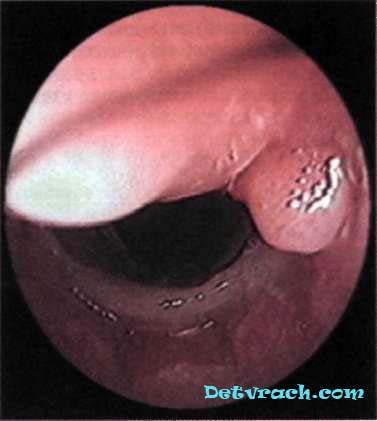
Рис. 1. Бронхоскопия больного Г., 26 лет, с Рубцовым стенозом трахеи после ее термического ожога. Грануляции у проксимального конца эндотрахеального стента.
Тем не менее, мы считаем целесообразным включать лазерное излучение только на фоне апноэ, что уменьшает концентрацию кислорода в просвете дыхательных путей в момент эвапорации и к тому же делает объект неподвижным. Кроме того, мы категорически не рекомендуем применять лазерное излучение при наличии в просвете дыхательных путей трубок, стентов, катетеров и т. д., например удалять лазером грануляции у концов стента.
Газ или воздух, проходящий внутри оболочки световода, сдувает дым и частички обугленной ткани с его конца. При этом улучшается видимость во время операции и меньше подгорают концы световодов. Следует заметить, что использование углекислого газа для охлаждения световодов при выполнении бронхофиброскопии под местной анестезией вызывает у больных неудержимый кашель. В таких случаях единственно возможной является продувка световодов атмосферным воздухом с помощью компрессора.
Еще одно осложнение связано с использованием бронхо-фиброскопа в качестве проводника для лазерного световода. При значительном изгибе дистального конца бронхофиброскопа вместе с проведенным по его каналу световодом во время лазерной эвапорации опухоли верхнедолевого бронха внезапно прогорела оболочка световода в области максимального изгиба и был так сильно поврежден тубус бронхофиброскопа, что потребовалась его полная замена. С тех пор мы стараемся как можно реже использовать бронхофиброскопы при лазерных операциях и тщательно контролируем степень изгиба световода.
Анестезиологические осложнения, возникающие во время бронхоскопических оперативных вмешательств, мало чем отличаются от таковых при диагностических и лечебных бронхоскопиях и подробно описаны нами ранее.
Необходимо еще раз отметить, что эндоскопические операции на трахее, как правило, сопровождаются более значительной травмой и требуют добавления местной анестезии в оперируемой области. Без этого возрастает частота ларингоспазма и мучительного кашля в момент пробуждения больного и в послеоперационном периоде.
