Открытие метода вакцинации дало старт новой эре борьбы с болезнями.
В состав прививочного материала входят убитые или сильно ослабленные микроорганизмы либо их компоненты (части). Они служат своеобразным муляжом, обучающим иммунную систему давать правильный ответ инфекционным атакам. Вещества, входящие в состав вакцины (прививки), не способны вызвать полноценное заболевание, но могут дать возможность иммунитету запомнить характерные признаки микробов и при встрече с настоящим возбудителем быстро его определить и уничтожить.
Производство вакцин получило массовые масштабы в начале ХХ века, после того как фармацевты научились обезвреживать токсины бактерий. Процесс ослабления потенциальных возбудителей инфекций получил название аттенуации.
Сегодня медицина располагает более, чем 100 видами вакцин от десятков инфекций.
Препараты для иммунизации по основным характеристикам делятся на три основных класса.
- Живые вакцины. Защищают от полиомиелита, кори, краснухи, гриппа, эпидемического паротита, ветряной оспы, туберкулеза, ротавирусной инфекции. Основу препарата составляют ослабленные микроорганизмы - возбудители болезней. Их сил недостаточно для развития значительного недомогания у пациента, но хватает, чтобы выработать адекватный иммунный ответ.
- Инактивированные вакцины. Прививки против гриппа, брюшного тифа, клещевого энцефалита, бешенства, гепатита А, менингококковой инфекции и др. В составе мертвые (убитые) бактерии или их фрагменты.
- Анатоксины (токсоиды). Особым образом обработанные токсины бактерий. На их основе делают прививочный материал от коклюша, столбняка, дифтерии.
В последние годы появился еще один вид вакцин - молекулярные. Материалом для них становятся рекомбинантные белки или их фрагменты, синтезированные в лабораториях путем применения методов генной инженерии (рекомбининтная вакцина против вирусного гепатита В).
Схемы изготовления некоторых видов вакцин
Живые бактериальные
Схема подходит для вакцины БЦЖ, БЦЖ-М.
Живые противовирусные

Схема подходит для производства вакцин от гриппа, ротавируса, герпеса I и II степеней, краснухи, ветряной оспы.
Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться:
- куриные эмбрионы;
- перепелиные эмбриональные фибробласты;
- первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков);
- перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293).
Первичный сырьевой материал очищают от клеточного дебриса в центрифугах и с помощью сложных фильтров.
Инактивированные антибактериальные вакцины
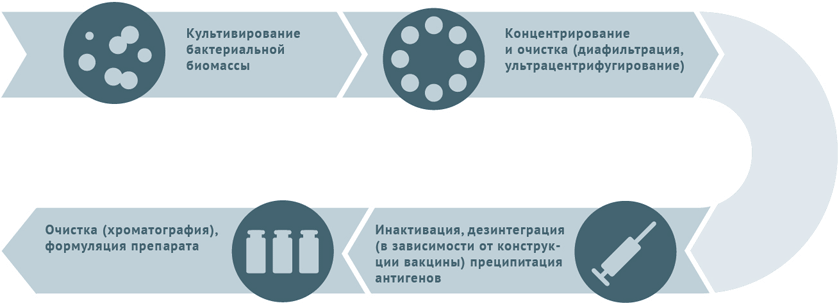
- Культивация и очистка штаммов бактерий.
- Инактивация биомассы.
- Для расщепленных вакцин клетки микробов дезинтегрируют и осаждают антигены с последующим их хроматографическим выделением.
- Для конъюгированных вакцин полученные при предыдущей обработке антигены (как правило, полисахаридные) сближают с белком-носителем (конъюгация).
Инактивированные противовирусные вакцины

- Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться куриные эмбрионы, перепелиные эмбриональные фибробласты, первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков), перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293). Первичная очистка для удаления клеточного дебриса проводится методами ультрацентрифугирования и диафильтрации.
- Для инактивации используются ультрафиолет, формалин, бета-пропиолактон.
- В случае приготовления расщепленных или субъединичных вакцин полупродукт подвергают действию детергента с целью разрушить вирусные частицы, а затем выделяют специфические антигены тонкой хроматографией.
- Человеческий сывороточный альбумин применяется для стабилизации полученного вещества.
- Криопротекторы (в лиофилизатах): сахароза, поливинилпирролидон, желатин.
Схема подходит для производства прививочного материала против гепатита А, желтой лихорадки, бешенства, гриппа, полиомиелита, клещевого и японского энцефалитов.
Анатоксины

Для дезактивации вредного воздействия токсинов используют методы:
- химический (обработка спиртом, ацетоном или формальдегидом);
- физический (подогрев).
Схема подходит для производства вакцин против столбняка и дифтерии.
По данным Всемирной Организации Здравоохранения (ВОЗ), на долю инфекционных заболеваний приходится 25 % от общего количества смертей на планете ежегодно. То есть инфекции до сих пор остаются в списке главных причин, обрывающих жизнь человека.
Одним из факторов, способствующих распространению инфекционных и вирусных заболеваний, являются миграция потоков населения и туризм. Перемещение человеческих масс по планете влияет на уровень здоровья нации даже в таких высокоразвитых странах, как США, ОАЭ и государства Евросоюза.
По материалам: «Наука и жизнь» № 3, 2006, «Вакцины: от Дженнера и Пастера до наших дней», академик РАМН В. В. Зверев, директор НИИ вакцин и сывороток им. И. И. Мечникова РАМН.
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Вопросы и ответы
Вакцина "Менюгейт" зарегистрирована в России? С какого возраста разрешена к применению?
Да, зарегистрирована, вакцина – от менингококка С, сейчас также есть вакцина конъюгированная, но уже против 4 типов менингококков – А, С, Y, W135 – Менактра. Прививки проводят с 9 мес.жизни.
Муж транспортировал вакцину РотаТек в другой город.Покупая ее в аптеке мужу посоветовали купить охлаждающий контейнер,и перед поездкой его заморозить в морозильной камере,потом привязать вакцину и так ее транспортировать. Время в пути заняло 5 часов. Можно ли вводить такую вакцину ребенку? Мне кажется,что если привязать вакцину к замороженному контейнеру, то вакцина замерзнет!
Отвечает Харит Сусанна Михайловна
Вы абсолютно правы, если в контейнере был лед. Но если там была смесь воды и льда- вакцина не должна замерзать. Однако живые вакцины, к которым относится ротавирусная, не увеличивают реактогенность при температуре менее 0, в отличие от неживых, а, например, для живой полиомиелитной допускается замораживание до -20 град С.
Моему сыну сейчас 7 месяцев.
В 3 месяца у него случился отек Квинке на молочную смесь Малютка.
Прививку от гепатита сделали в роддоме, вторую в два месяца и третью вчера в семь месяцев. Реакция нормальная, даже без температуры.
Но вот на прививку АКДС нам устно дали медотвод.
Я за прививки!! И хочу сделать прививку АКДС. Но хочу сделать ИНФАНРИКС ГЕКСА. Живем в Крыму!!! В крыму ее нигде нет. Посоветуйте как поступить в такой ситуации. Может есть зарубежный аналог? Бесплатную делать категорически не хочу. Хочу качественную очищеную, что бы как монжно меньше риска!!!
В Инфанрикс Гекса содержится компонент против гепатита В. Ребенок полностью привит против гепатита. Поэтому в качестве зарубежного аналога АКДС можно сделать вакцину Пентаксим. Кроме того, следует сказать, что отек Квинке на молочную смесь не является противопоказанием к вакцине АКДС.
Подскажите, пожалуйста, на ком и как тестируют вакцины?
Отвечает Полибин Роман Владимирович
Как и все лекарственные препараты вакцины проходят доклинические исследования (в лаборатории, на животных), а затем клинические на добровольцах (на взрослых, а далее на подростках, детях с разрешения и согласия их родителей). Прежде чем разрешить применение в национальном календаре прививок исследования проводят на большом числе добровольцев, например вакцина против ротавирусной инфекции испытывалась почти на 70 000 в разных странах мира.
Почему на сайте не представлен состав вакцин? Почему до сих пор проводится ежегодная реакция Манту (зачастую не информативна), а не делается анализ по крови, например, квантифероновый тест? Как можно утверждать реакции иммунитета на введенную вакцину, если еще ни кому не известно в принципе, что такое иммунитет и как он работает, особенно если рассматривать каждого отдельно взятого человека?
Отвечает Полибин Роман Владимирович
Состав вакцин изложен в инструкциях к препаратам.
Реакция Манту. По Приказу № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерациии» и Санитарным правилам СП 3.1.2.3114-13 "Профилактика туберкулеза", несмотря на наличие новых тестов, детям необходимо ежегодно делать реакцию Манту, но так как этот тест может давать ложноположительные результаты, то при подозрении на тубинфицирование и активную туберкулезную инфекцию проводят Диаскин-тест. Диаскин-тест является высоко чувствительным (эффективным) для выявления активной туберкулезной инфекции (когда идет размножение микобактерий). Однако полностью перейти на Диаскин-тест и не делать реакцию Манту фтизиатры не рекомендуют, так как, он не "улавливает" раннее инфицирование, а это важно, особенно для детей, поскольку профилактика развития локальных форм туберкулеза эффективна именно в раннем периоде инфицирования. Кроме того, инфицирование микобактерией туберкулеза необходимо определять для решения вопроса о ревакцинации БЦЖ. К сожалению, нет ни одного теста, который бы со 100% точностью ответил на вопрос, есть инфицирование микобактерией или заболевание. Квантифероновый тест также выявляет только активные формы туберкулеза. Поэтому при подозрении на инфицирование или заболевание (положительная реакция Манту, контакт с больным, наличие жалоб и пр.) используются комплексные методы (диаскин-тест, квантифероновый тест, рентгенография и др.).
Что касается «иммунитета и как он работает», в настоящее время иммунология - это высокоразвитая наука и многое, в частности, что касается процессов на фоне вакцинации – открыто и хорошо изучено.
Ребёнку 1 год и 8 месяцев, все прививки ставились в соответствии с календарем прививок. В том числе 3 пентаксима и ревакцинация в полтора года тоже пентаксим. В 20 месяцев надо ставить от полиомиелита. Очень всегда переживаю и отношусь тщательно к выбору нужных прививок, вот и сейчас перерыла весь интернет, но так и не могу решить. Мы ставили всегда инъекцию (в пентаксиме). А теперь говорят капли. Но капли-живая вакцина, я боюсь различных побочек и считаю, что лучше перестраховаться. Но вот читала, что капли от полиомиелита вырабатывают больше антител, в том числе и в желудке, то есть более эффективные, чем инъекция. Я запуталась. Поясните, инъекция менее эффективна (имовакс-полио, например)? Отчего ведутся такие разговоры? У каплей боюсь хоть и минимальный, но риск осложнения в виде болезни.
Отвечает Полибин Роман Владимирович
В настоящее время Национальный календарь прививок России предполагает комбинированную схему вакцинации против полиомиелита, т.е. только 2 первых введения инактивированной вакциной и остальные – оральной полиовакциной. Это связано с тем, чтобы полностью исключить риск развития вакциноассоциированного полиомиелита, который возможен только на первое и в минимальном проценте случаев на второе введение. Соответственно, при наличии 2-х и более прививок от полиомиелита инактивированной вакциной, осложнения на живую полиовакцину исключены. Действительно, считалось и признается некоторыми специалистами, что оральная вакцина имеет преимущества, так как формирует местный иммунитет на слизистых кишечника в отличие от ИПВ. Однако сейчас стало известно, что инактивированная вакцина в меньшей степени, но также формирует местный иммунитет. Кроме того, 5 введений вакцины против полиомиелита как оральной живой, так и инактивированной вне зависимости от уровня местного иммунитета на слизистых оболочках кишечника, полностью защищают ребенка от паралитических форм полиомиелита. В связи с вышесказанным вашему ребенку необходимо сделать пятую прививку ОПВ или ИПВ.
Следует также сказать, что на сегодняшний день идет реализация глобального плана Всемирной организации здравоохранения по ликвидации полиомиелита в мире, которая предполагает полный переход всех стран к 2019 году на инактивированную вакцину.
В нашей стране уже очень долгая история использования многих вакцин – ведутся ли долгосрочные исследования их безопасности и можно ли ознакомиться с результатами воздействия вакцин на поколения людей?
Отвечает Шамшева Ольга Васильевна
За прошлый век продолжительность жизни людей возросла на 30 лет, из них 25 дополнительных лет жизни люди получили за счет вакцинации. Больше людей выживают, они живут дольше и качественнее за счет того, что снизилось инвалидность из-за инфекционных заболеваний. Это общий ответ на то, как влияют вакцины на поколения людей.
На сайте Всемирной Организации Здравоохранения (ВОЗ) есть обширный фактический материал о благотворном влиянии вакцинации на здоровье отдельных людей и человечества в целом. Отмечу, что вакцинация –это не система верований, это - область деятельности, опирающаяся на систему научных фактов и данных.
На основании чего мы можем судить о безопасности вакцинации? Во-первых, ведется учет и регистрация побочных действий и нежелательных явлений и выяснение их причинно-следственной связи с применением вакцин (фармаконадзор). Во-вторых, важную роль в отслеживании нежелательных реакций играют постмаркетинговые исследования (возможного отсроченного неблагоприятного действия вакцин на организм), которые проводят компании - владельцы регистрационных свидетельств. И, наконец, проводится оценка эпидемиологической, клинической и социально-экономической эффективности вакцинации в ходе эпидемиологических исследований.
Что качается фармаконадзора, то у нас в России система фармаконадзора только формируется, но демонстрирует очень высокие темпы развития. Только за 5 лет число зарегистрированных сообщений о нежелательных реакциях на лекарственные средства в подсистему «Фармаконадзор» АИС Росздравнадзора выросло в 159 раз. 17 033 жалобы в 2013 году против 107 в 2008. Для сравнения – в США в год обрабатываются данные около 1 млн случаев. Система фармаконадзора позволяет отслеживать безопасность препаратов, накапливаются статистические данные, на основании которых может измениться инструкция по медицинскому применению препарата, препарат может быть отозван с рынка и т.п. Таким образом, обеспечивается безопасность пациентов.
И по закону «Об обращении лекарственных средств» от 2010 года врачи обязаны сообщать федеральным органам контроля обо всех случаях побочного действия лекарственных средств.
На протяжении столетий человечество пережило не одну эпидемию, унёсшую жизни многих миллионов людей. Благодаря современной медицине удалось разработать препараты, позволяющие избежать множества смертельных заболеваний. Эти препараты носят название "вакцина" и подразделяются на несколько видов, которые мы опишем в этой статье.
Что такое вакцина и как она работает?
Вакцина - это медицинский препарат, содержащий убитые или ослабленные возбудители различных заболеваний либо синтезированные белки патогенных микроорганизмов. Их вводят в организм человека для создания иммунитета к определённой болезни.
Введение вакцин в человеческий организм называется вакцинация, или прививка. Вакцина, попадая в организм, побуждает иммунную систему человека вырабатывать специальные вещества для уничтожение возбудителя, тем самым формируя у него избирательную память к болезни. Впоследствии, если человек инфицируется этим заболеванием, его иммунная система окажет быстрое противодействие возбудителю и человек не заболеет вовсе или перенесет легкую форму болезни.
Способы вакцинации
Иммунобиологические препараты могут вводиться различными способами согласно инструкции к вакцинам в зависимости от вида препарата. Бывают следующие способы вакцинации.

- Введение вакцины внутримышечно. Местом прививки у детей до года является верхняя поверхность середины бедра, а детям с 2 лет и взрослым предпочтительнее вводить препарат в дельтовидную мышцу, которая находится в верхней части плеча. Способ применим, когда нужна инактивированная вакцина: АКДС, АДС, против вирусного гепатита В и противогриппозная вакцина.

Отзывы родителей говорят о том, что дети младенческого возраста лучше переносят вакцинацию в верхнюю часть бедра, нежели в ягодицу. Этого же мнения придерживаются и медики, обуславливая это тем, что в ягодичной области может быть аномальное размещение нервов, встречаемое у 5 % детей до года. К тому же в ягодичной области у детей этого возраста имеется значительный жировой слой, что увеличивает вероятность попадания вакцины в подкожный слой, из-за чего снижается эффективность препарата.
- Подкожные инъекции вводятся тонкой иглой под кожу в области дельтовидной мышцы или предплечья. Пример - БЦЖ, прививка от оспы.

- Интраназальный способ применим для вакцин в форме мази, крема или спрея (прививка от кори, краснухи).
- Пероральный способ - это когда вакцину в виде капель помещают в рот пациенту (полиомиелит).

Виды вакцин
Сегодня в руках медицинских работников в борьбе с десятками инфекционных заболеваний имеется более ста вакцин, благодаря которым удалось избежать целых эпидемий и значительно улучшить качество медицины. Условно принято выделять 4 вида иммунобиологических препаратов:
- Живая вакцина (от полиомиелита, краснухи, кори, эпидемического паротита, гриппа, туберкулёза, чумы, сибирской язвы).
- Инактивированная вакцина (против коклюша, энцефалита, холеры, менингококковой инфекции, бешенства, брюшного тифа, гепатита А).
- Анатоксины (вакцины против столбняка и дифтерии).
- Молекулярные или биосинтетические вакцины (от гепатита В).
Типы вакцин
Вакцины также можно группировать по признаку состава и способа их получения:
- Корпускулярные, то есть состоящие из цельных микроорганизмов возбудителя.
- Компонентные или бесклеточные состоят из частей возбудителя, так называемого антигена.
- Рекомбинантные: в состав этой группы вакцин входят антигены патогенного микроорганизма, введённые с помощью методов генной инженерии в клетки другого микроорганизма. Представителем данной группы является вакцина от гриппа. Еще яркий пример - вакцина от вирусного гепатита В, которая получается путём введения антигена (HBsAg) в клетки дрожжевых грибов.
Ещё один критерий, по которому классифицируется вакцина, - это количество профилактируемых ею заболеваний или возбудителей:
- Моновалентные вакцины служат для профилактики только одного заболевания (например, вакцина БЦЖ против туберкулёза).
- Поливалентные или ассоциированные - для прививки от нескольких болезней (пример - АКДС против дифтерии, столбняка и коклюша).
Живая вакцина
Живая вакцина - это незаменимый препарат для профилактики множества инфекционных заболеваний, который встречается только в корпускулярном виде. Характерной особенностью этого вида вакцины считается то, что главным её компонентом являются ослабленные штаммы возбудителя инфекции, способные размножаться, однако генетически лишённые вирулентности (способности заражать организм). Они способствуют выработке организмом антител и иммунной памяти.
Преимущество живых вакцин состоит в том, что ещё живые, но ослабленные возбудители побуждают человеческий организм вырабатывать длительную невосприимчивость (иммунитет) к данному патогенному агенту даже при однократной вакцинации. Существует несколько способов введения вакцины: внутримышечно, под кожу, капли в нос.
Недостаток - возможна генная мутация патогенных агентов, что приведет к заболеванию привитого. В связи с этим противопоказана для пациентов с особо ослабленным иммунитетом, а именно для людей с иммунодефицитом и онкобольных. Требует особых условий транспортировки и хранения препарата с целью обеспечения сохранности живых микроорганизмов в нём.
Инактивированные вакцины
Применение вакцин с инактивированными (мёртвыми) патогенными агентами широко распространено для профилактики вирусных заболеваний. Принцип действия базируется на введении в организм человека искусственно культивированных и лишённых жизнеспособности вирусных возбудителей.
«Убитые» вакцины по составу могут быть как цельномикробными (цельновиральными), так и субъединичными (компонентными) и генно-инженерными (рекомбинантными).
Важным преимуществом «убитых» вакцин является их абсолютная безопасность, то есть отсутствие вероятности инфицирования привитого и развития инфекции.
Недостаток - более низкая продолжительность иммунной памяти по сравнению с «живыми» прививками, также у инактивированных вакцин сохраняется вероятность развития аутоиммунных и токсических осложнений, а для формирования полноценной иммунизации требуется несколько процедур вакцинации с выдерживанием необходимого интервала между ними.
Анатоксины
Анатоксины - это вакцины, созданные на основе обеззараженных токсинов, выделяемых в процессе жизнедеятельности некоторыми возбудителями инфекционных заболеваний. Особенность этой прививки состоит в том, что она провоцирует формирование не микробной невосприимчивости, а антитоксического иммунитета. Таким образом, анатоксины с успехом используются для профилактики тех заболеваний, у которых клинические симптомы связаны с токсическим эффектом (интоксикацией), возникающим в результате биологической активности патогенного возбудителя.
Форма выпуска - прозрачная жидкость с осадком в стеклянных ампулах. Перед применением нужно встряхнуть содержимое для равномерного распределения анатоксинов.
Преимущества анатоксинов - незаменимы для профилактики тех заболеваний, против которых живые вакцины бессильны, к тому же они более устойчивы к колебаниям температуры, не требуют специальных условий для хранения.
Недостатки анатоксинов - индуцируют только антитоксический иммунитет, что не исключает возможности возникновения локализованных болезней у привитого, а также носительство им возбудителей данного заболевания.
Изготовление живых вакцин
Массово вакцину начали изготовлять в начале XX века, когда биологи научились ослаблять вирусы и патогенные микроорганизмы. Живая вакцина - это около половины всех профилактических препаратов, применяемых мировой медициной.

Производство живых вакцин базируется на принципе пересева возбудителя в невосприимчивый или маловосприимчивый к данному микроорганизму (вирусу) организм либо культивирование возбудителя в неблагоприятных для него условиях с воздействием на него физических, химических и биологических факторов с последующим отбором невирулентных штаммов. Чаще всего субстрактом для культивирования авирулентных штаммов служат эмбрионы курицы, первичные клеточные (эбриональные фибробласты курицы или перепёлки) и перевиваемые культуры.
Получение «убитых» вакцин
Производство инактивированных вакцин от живых отличается тем, что их получают путём умерщвления, а не аттенуации возбудителя. Для этого отбираются только те патогенные микроорганизмы и вирусы, которые обладают наибольшей вирулентностью, они должны быть одной популяции с чётко очерченными характерными для неё признаками: форма, пигментация, размеры и т. д.
Инактивация колоний возбудителя осуществляется несколькими способами:
- перегревом, то есть воздействием на культивируемый микроорганизм повышенной температурой (56-60 градусов) определённое время (от 12 минут до 2 часов);
- воздействие формалином в течение 28-30 суток с поддержанием температурного режима на уровне 40 градусов, инактивирующим химическим реактивом может также выступать раствор бета-пропиолактона, спирта, ацетона, хлороформа.
Изготовление анатоксинов
Для того чтобы получить токсоид, вначале культивируют токсогенные микроорганизмы в питательной среде, чаще всего жидкой консистенции. Это делается для того, чтобы накопить в культуре как можно больше экзотоксина. Следующий этап - это отделение экзотоксина от клетки-продуцента и его обезвреживание при помощи тех же химических реакций, что применяются и для «убитых» вакцин: воздействие химических реактивов и перегрева.
Для снижения реагентности и восприимчивости антигены очищают от балласта, концентрируют и адсорбируют окисью алюминия. Процесс адсорбции антигенов играет важную роль, поскольку введённая инъекция с большой концентрацией токсоидов формирует депо антигенов, в результате антигены поступают и разносятся по организму медленно, обеспечивая тем самым эффективный процесс иммунизации.
Уничтожение неиспользованной вакцины

Независимо от того, какие вакцины были использованы для прививки, ёмкости с остатками препаратов нужно обработать одним из следующих способов:
- кипячение использованных ёмкостей и инструментария в течение часа;
- дезинфекция в растворе 3-5%-ного хлорамина в течение 60 минут;
- обработка 6%-ной перекисью водорода также в течение 1 часа.
Препараты с истекшим сроком годности нужно непременно направить в районный санэпидцентр для утилизации.
Вакцины (определение, классификация которых рассмотрены в данной статье) представляют собой иммунологические средства, применяемые в качестве активной иммунопрофилактики (иначе - для формирования активной стойкой невосприимчивости организма к данному конкретному возбудителю). По заключению ВОЗ, вакцинация - оптимальный метод профилактики инфекционных патологий. Благодаря высокой эффективности, простоте метода, возможности широкого охвата вакцинируемого населения для массового предупреждения патологий, иммунопрофилактика во многих странах отнесена к разряду государственных приоритетов.
Вакцинация
Вакцинация - это специальные профилактические меры, направленные на защиту ребенка либо взрослого от некоторых патологий полностью либо значительно снижающие их появления при возникновении.
Подобный эффект достигается за счет "обучения" иммунитета. При введении препарата организм (точнее его иммунная система) борется с искусственно введенной инфекцией и "запоминает" ее. При повторной инфекции иммунитет активируется гораздо быстрее и полностью уничтожает чужеродные агенты.
Перечень проводимых мероприятий по вакцинации включает в себя:
- отбор подлежащих вакцинации лиц;
- выбор препарата;
- формирование схемы применения вакцины;
- контроль эффективности;
- терапия (при необходимости) вероятных осложнений и патологических реакций.
Способы вакцинации
- Внутрикожный. Примером может служить БЦЖ. Введение производят в плечо (наружную его треть). Подобный метод применяется также для профилактики туляремии, чумы, бруцеллеза, язвы сибирской, лихорадки Ку.
- Пероральный. Применяется для профилактики полиомиелита и бешенства. На стадиях разработки пероральные средства от гриппа, кори, тифа брюшного, менингококковой инфекции.
- Подкожный. При данном способе не сорбированный препарат вводится в подлопаточную либо плечевую (наружная поверхность на границе средней и верхней третей плеча) область. Преимущества: низкая аллергенность, простота введения, стойкость иммунитета (как местного, так и общего).
- Аэрозольный. Применяется в качестве экстренной иммунизации. Высокоэффективными являются аэрозольные средства против бруцеллеза, гриппа, туляремии, дифтерии, язвы сибирской, коклюша, чумы, краснухи, газовой гангрены, туберкулеза, столбняка, тифа брюшного, ботулизма, дизентерии, паротита В.
- Внутримышечный. Производится в мускулы бедра (в верхнюю передненаружную часть четырехглавой бедренной мышцы). Например, АКДС.

Современная классификация вакцин
Существует несколько подразделений вакцинных препаратов.
1. Классификация средств в соответствии с поколением:
- 1 поколение (корпускулярные вакцины). В свою очередь, делятся на аттенуированные (ослабленные живые) и инактивированные (убитые) средства;
- 2 поколение: субъединичные (химические) и обезвреженные экзотоксины (анатоксины);
- 3 поколение представлено рекомбинантными и рекомбинантными вакцинами от бешенства;
- 4 поколение (еще не включено в практику), представлено плазмидными ДНК, синтетическими пептидами, растительными вакцинами, вакцинами, что содержат продукты ГКГ и антиидиотипическими препаратами.

2. Классификация вакцин (микробиология также делит их на несколько классов) по происхождению. По происхождению вакцины делятся на:
- живые, что изготовлены из живых, но ослабленных микроорганизмов;
- убитые, созданные на основе инактивированных различными способами микроорганизмов;
- вакцины химического происхождения (на базе высокоочищенных антигенов);
- вакцины, что созданы с помощью биотехнологических методик, в свою очередь подразделяются на:
Вакцины синтетические на базе олигосахаридов и олигопептидов;
ДНК-вакцины;
Вакцины генно-инженерные, созданные на базе продуктов, образующихся в результате синтеза рекомбинантных систем.
3. В соответствии с входящими в состав препаратов Аг, существует следующая классификация вакцин (то есть в качестве Аг в вакцинах могут присутствовать):
- целые микробные клетки (инактивированные либо живые);
- отдельные компоненты микробных тел (чаще протективные Аг);
- микробные токсины;
- созданные синтетическим путем Аг микробов;
- Аг, что получены с помощью методик генной инженерии.
В зависимости от способностей вырабатывать нечувствительность к нескольким либо одному агенту:
- моновакцины;
- поливакцины.
Классификация вакцин в соответствие с набором Аг:
- компонентные;
- корпускулярные.
Живые вакцины
Для изготовления подобных вакцин используют ослабленные штаммы инфекционных агентов. Подобные вакцины имеют иммуногенные свойства, однако возникновения симптоматики болезни при иммунизации, как правило, не вызывают.
В результате проникновения живой вакцины в организм формируется стойкий клеточный, секреторный, гуморальный иммунитет.

Плюсы и минусы
Преимущества (классификация, применение рассмотрены в этой статье):
- необходима минимальная дозировка;
- возможность разнообразных способов вакцинации;
- быстрое вырабатывание иммунитета;
- высокая эффективность;
- низкая цена;
- иммуногенность максимально естественная;
- в составе отсутствуют консерванты;
- под воздействием таких вакцин активируются все типы иммунитета.
Отрицательные стороны:
- в случае наличия у пациента ослабленного иммунитета при введении живой вакцины возможно развитие болезни;
- вакцины такого типа крайне чувствительны к перепадам температур, а потому при введении "испорченной" живой вакцины развиваются негативные реакции либо вакцина полностью теряет свои свойства;
- невозможность комбинирования подобных вакцин с другими вакцинными препаратами, ввиду развития побочных реакций либо потери терапевтической эффективности.
Классификация живых вакцин
Выделяют следующие типы живых вакцин:
- Аттенуированные (ослабленные) вакцинные препараты. Их производят из штаммов, что имеют сниженную патогенность, но выраженную иммуногенность. При введении вакцинного штамма в организме развивается подобие инфекционного процесса: инфекционные агенты размножаются, тем самым вызывая формирование иммунных реакций. Среди подобных вакцин наиболее известны препараты для профилактики тифа брюшного, язвы сибирской, Ку-лихорадки и бруцеллеза. Но все же основная часть живых вакцин - противовирусные препараты от аденовирусных инфекций, желтой лихорадки, Сэйбина (против полиомиелита), краснухи, кори, гриппа;
- Вакцины дивергентные. Их изготавливают на базе родственных возбудителей инфекционных патологий штаммов. Их антигены провоцируют возникновение иммунного ответа, перекрестно направленного на антигены возбудителя. Примером подобных вакцин является вакцина-профилактика против оспы натуральной, что изготовлена на базе вируса оспы коровьей и БЦЖ, на базе микобактерий, вызывающих бычий туберкулез.

Вакцины от гриппа
В качестве наиболее эффективной профилактики гриппа применяются вакцины. Они представляют собой биологические препараты, что обеспечивают возникновение краткосрочной устойчивости к вирусам гриппа.
Показаниями для подобной вакцинации являются:
- возраст 60 лет и старше;
- бронхолегочные хронические либо сердечно-сосудистые патологии;
- беременность (2-3 триместры);
- персонал амбулаторий и стационаров;
- лица, постоянно пребывающие в закрытых коллективах (тюрьмы, общежития, дома престарелых и так далее);
- пациенты, находящиеся на стационарном либо амбулаторном лечении, что имеют гемоглабинопатии, иммуносупрессии, патологии печени, почек и метаболические расстройства.

Разновидности
Классификация вакцин от гриппа включает в себя следующие группы:
- Вакцины живые;
- Вакцины инактивированные:
- вакцины цельновирионные. Включают неразрушенные высокоочищенные инактивированные вирионы;
- ращепленные (сплит-вакцины). Например: "Флюарикс", "Бегривак", "Ваксигрип". Созданы на базе разрушенных гриппозных вирионов (всех белков вируса);

- вакцины субъединичные ("Агриппал", "Гриппол", "Инфлювак") имеют в составе два вирусных поверхностных белка, нейраминидазы и гемагглютинина, обеспечивающие индукцию иммунного ответа при гриппе. Иные белки вириона, а также куриного эмбриона отсутствуют, так как устраняются во время очистки.
Материал из WikiDOL
СОСТАВИТЕЛИ : д. м. н., проф. М.А. Горбунов, д. м. н., проф. Н.Ф. Никитюк, к. м. н. Г.А. Ельшина, к. м. н. В.Н. Икоев, к. м. н. Н.И. Лонская, к. б. н. К.М. Мефед, М.В. Соловьева, ФГБУ «НЦЭСМП» Минздравсоцразвития России, Центр экспертизы и контроля ИЛП
Вакцины - это препараты, получаемые из живых аттенуированных штаммов или убитых культур микроорганизмов и их антигенов, предназначенные для создания активного иммунного ответа в организме привитых людей и животных.
Среди различных групп медицинских биологических препаратов, применяемых для иммунопрофилактики и иммунотерапии инфекционных болезней, вакцины являются наиболее эффективным средством предупреждения инфекционных заболеваний. Основным действующим началом каждой вакцины является иммуноген, по структуре аналогичный компонентам возбудителя заболевания, ответственным за выработку иммунитета.
В зависимости от природы иммуногена вакцины подразделяются на:
- живые;
- убитые (инактивированные);
- расщепленные (сплит-вакцины);
- субъединичные (химические) вакцины;
- анатоксины;
- рекомбинантные;
- конъюгированные;
- виросомальные;
- вакцины с искусственным адъювантом;
- комбинированные (ассоциированные поливакцины).
Живые вакцины
Живые вакцины содержат ослабленные живые микроорганизмы (бактерии, вирусы, риккетсии), созданные на основе апатогенных возбудителей, аттенуированных в искусственных или естественных условиях, путем инактивации генов или за счет их мутаций. Живые вакцины создают устойчивый и длительный иммунитет, по напряженности приближающийся к постинфекционному иммунитету, при этом для выработки иммунитета, как правило, достаточно однократного введения препарата. Вакцинный инфекционный процесс продолжается несколько недель, не сопровождается клинической картиной заболевания и приводит к формированию специфического иммунитета.
Убитые (инактивированные) вакцины
Убитые вакцины готовятся из инактивированных вирулентных штаммов бактерий и вирусов и содержат убитый целый микроорганизм, или компоненты клеточной стенки и других частей возбудителя, обладающих полным набором необходимых антигенов. Для инактивации возбудителей применяют физические (температура, радиация, УФ-лучи) или химические (спирт, ацетон, формальдегид) методы, которые обеспечивают минимальное повреждение структуры антигенов. Эти вакцины обладают более низкой иммунологической эффективностью, по сравнению с живыми вакцинами, поэтому вакцинация проводится, в основном, в 2 или 3 приема и требует ревакцинации, что формирует достаточно стойкий иммунитет, предохраняя привитых от заболевания или уменьшая его тяжесть.
Расщепленные (сплит-вакцины)
Вакцины содержат разрушенные инактивированные вирионы, при этом сохраняя все белки вируса (поверхностные и внутренние). За счет высокой очистки от вирусных липидов и белков куриного эмбриона, субстрата культивирования сплит-вакцины имеют низкую реактогенность. Высокая степень специфической безопасности и достаточная иммуногенность позволяют их применение среди детей с 6-месячного возраста и беременных женщин.
Субъединичные (химические) вакцины
Субъединичные вакцины состоят из отдельных антигенов микроорганизма, способных обеспечить надежный иммунный ответ у привитого. Для получения протек-тивных антигенов преимущественно используются различные химические методы с последующей очисткой полученного материала от балластных веществ. Применение адъювантов усиливает эффективность вакцин. субъединичные (химические) вакцины обладают слабой реактогенностью, могут вводиться в больших дозах и многократно, а также применяться в различных ассоциациях, направленных одновременно против ряда инфекций.
Анатоксины
Анатоксины готовятся из микробных экзотоксинов, утративших токсичность в результате обезвреживания формальдегидом при нагревании, но сохранивших видовые антигенные свойства и способность вызывать образование антител (антитоксинов). Очищенный от балластных веществ и концентрированный анатоксин сорбируют на гидроксиде алюминия. Анатоксины формируют антитоксический иммунитет, который слабее постинфекционного иммунитета.
Рекомбинантные вакцины (векторные)
Рекомбинантные вакцины получают клонированием генов, обеспечивающих синтез необходимых антигенов, введением этих генов в вектор и в клетки-продуценты (вирусы, бактерии, грибы и пр.), затем культивируют клетки in vitro, отделяют антиген и очищают его. Новая технология открыла широкие перспективы в создании вакцин. Рекомбинантные вакцины безопасны, достаточно эффективны, для их получения применяется высокоэффективная технология, они могут быть использованы для разработки комплексных вакцин, создающих иммунитет одновременно против нескольких инфекций.
Конъюгированные вакцины
Вакцины представляют собой конъюгаты полисахарида, полученного из возбудителей инфекции и белкового носителя (дифтерийного или столбнячного анатоксина). Полисахариды-антигены обладают слабой иммуногенностью и слабой способностью к формированию иммунологической памяти. связывание полисахаридов с белковым носителем, хорошо распознаваемым иммунной системой, резко усиливает иммуногенные свойства конъюгата и вызывает протективный иммунитет .
Виросомальные вакцины
Виросомальные вакцины содержат инактивированный виросомальный комплекс, ассоциированный с высокоочищенными протективными антигенами. Виросомы выполняют функции носителя антигена и адъюванта, усиливая иммунный ответ, способный индуцировать как гуморальный, так и клеточный иммунитет.
Вакцины с искусственным адъювантом
Принцип создания таких вакцин заключается в использовании естественных антигенов возбудителей инфекционных заболеваний и синтетических носителей. Один из вариантов таких вакцин состоит из белкового антигена вируса и искусственного стимулятора (например, полиоксидония), обладающего выраженными адъювантными (повышающими иммуногенность антигенов) свойствами.
Комбинированные вакцины (ассоциированные поливакцины)
Данные вакцины представляют собой смесь штаммов разных видов возбудителей или их антигенов для профилактики двух и более инфекций. При разработке комбинированных вакцин учитывается совместимость не только антигенных компонентов, но и их различных добавок (адъювантов, консервантов, стабилизаторов и пр.). Это вакцины различных типов, содержащие несколько компонентов. Побочные реакции организма на ассоциированные вакцины возникают, как правило, несколько чаще, чем на моновакцины, но позволяют создавать защиту привитых в сжатые сроки от нескольких инфекционных болезней.
Актуальной задачей современной вакцинологии является постоянное совершенствование вакцинных препаратов, подходов к их применению, отработок схем, дозировок, методов и сроков введения среди различных возрастных групп.
Особенности технологии производства вакцины, а также механизм их действия при формировании иммунитета необходимо учитывать при организации и проведении всех этапов клинических испытаний.
До начала проведения клинических исследований, следует четко обосновать выбор территорий и контингентов для проведения планируемых исследований. с этой целью необходимо проведение ретроспективного эпидемиологического анализа инфекционного заболевания на определенной территории среди популяции, включаемой в протокол клинических испытаний. По результатам эпидемиологического анализа отбирают группы добровольцев по возрасту, полу, социальным характеристикам, в том числе территориальным и сезонным колебаниям заболеваемости, что крайне необходимо при планировании клинических испытаний и определения безопасности и эффективности различного вида вакцин.
Читайте также
- Общие положения проведения клинических исследований вакцин
- Клинические исследования инактивированных гриппозных вакцин
- Особенности проведения клинических исследований вакцин против ВИЧ/СПИД
- Особенности проведения клинических исследований вакцин против особо опасных инфекций
- Особенности проведения клинических исследований вакцин против кори, паротита и краснухи
Существуют различные типы вакцин, которые отличаются по способу производства активного компонента-антигена, на который вырабатывается иммунитет. От способа производства вакцин зависит способ введения, метод назначения и требования к хранению. В настоящее время различают 4 основных разновидности вакцин:
- Живые ослабленные вакцины
- Инактивированные (с убитым антигеном) вакцины
- Субъединичные (с очищенным антигеном)
- Вакцины с анатоксином (инактивированным токсином).
Как производят различные виды вакцин 1, 3 ?
Живые ослабленные (аттенуированные) вакцины - производят из ослабленных возбудителей заболеваний. Для того, чтобы добиться этого, бактерию или вирус размножают в неблагоприятных для него условиях, повторяя процесс до 50 раз.
Пример живых ослабленных вакцин против заболеваний:
- Туберкулеза
- Полиомиелита
- Ротавирусной инфекции
- Желтой лихорадки

Инактивированные (из убитых антигенов) вакцины - производят, убивая культуру возбудителя болезни. При этом такой микроорганизм не способен размножаться, но вызывает выработку иммунитета против заболевания.

Адаптировано с http://www.slideshare.net/addisuga/6-immunization-amha Accessed by May 2016
Пример инактивированных (из убитых антигенов) вакцин
- Цельноклеточная коклюшная вакцина
- Инактивированная полиомиелитная вакцина
Положительные и отрицательные особенности инактивированных (из убитых антигенов) вакцин

Адаптировано из Электронного тренинга ВОЗ. Основы безопасности вакцин.
Субъединичные вакцины
- так же, как и инактивированные, не содержат живого возбудителя. В состав таких вакцин входят лишь отдельные компоненты возбудителя, на которые вырабатывается иммунитет.
Субъединичные вакцины в свою очередь делятся на:
- Субъединичные вакцины с белковым носителем (грипп, бесклеточная вакцина против коклюша, гепатит В)
- Полисахаридные (против пневмококковой и менингококковой инфекции)
- Конъюгированные (против гемофильной, пневмококковой и менингококковой инфекции для детей с 9-12 мес.жизни).

Адаптировано с http://www.slideshare.net/addisuga/6-immunization-amha Accessed by May 2016

Адаптировано из Электронного тренинга ВОЗ. Основы безопасности вакцин.

Адаптировано с http://www.slideshare.net/addisuga/6-immunization-amha Accessed by May 2016
Примеры вакцин на основе анатоксинов:
- Против дифтерии
- Против столбняка

Адаптировано из Электронного тренинга ВОЗ. Основы безопасности вакцин.
Как вводятся различные виды вакцин 1 ?
В зависимости от вида, вакцины могут быть введены в организм человека различными способами.

Пероральный (через рот) - данный метод введения достаточно прост, так как не требуется использования игл и шприца. Например, вакцина оральная полиомиелитная (ОПВ), вакцина против ротавирусной инфекции.
Внутрикожная инъекция
- при таком виде введения вакцина вводится в самый верхний слой кожи.
Например, вакцина БЦЖ.
Подкожная инъекция
- при таком виде введения вакцина вводится между кожей и мышцей.
Например, вакцина против кори, краснухи и паротита (КПК).
Внутримышечная инъекция
- при таком виде введения вакцина вводится глубоко в мышцу.
Например, вакцина против коклюша, дифтерии и столбняка (АКДС), вакцина против пневмококковой инфекции.

Адаптировано с http://www.slideshare.net/addisuga/6-immunization-amha Accessed by May 2016
Какие еще компоненты входят в состав вакцин 1,2 ?
Знание о составе вакцин может помочь в понимании возможных причин возникновения поствакцинальных реакций, а также в выборе вакцины при наличии у человека аллергии или при непереносимости отдельных компонентов вакцин. Помимо чужеродных веществ (антигенов) возбудителей болезней в составе вакцин могут быть:
- Стабилизаторы
- Консерванты
- Вещества для усиления ответа иммунной системы (адъюванты)
Стабилизаторы
необходимы, чтобы помочь вакцине поддерживать свою эффективность при хранении. Стабильность вакцин крайне важна, так как из-за нарушения условий транспортировки и хранения вакцины может снизиться ее способность вызывать эффективную защиту против инфекции.
В качестве стабилизаторов в вакцинах могут быть использованы:
- Хлорид магния (MgCl2) – оральная полиомиелитная вакцина (ОПВ)
- Магния сульфат (MgSO4)- коревая вакцина
- Лактоза-сорбитол
- Сорбитол-желатин.
Консерванты
добавляются в вакцины, которые фасуются во флаконы, расчитанные на использование для нескольких человек одновременно (многодозовые), для предупреждения роста бактерий и грибов.
К консервантам, которые чаще всего используются в составе вакцин, относятся:
- Тиомерсал
- Фенол
- Феноксиэтанол.

- С 1930 года используется, как консервант в многодозовых флаконах вакцин, которые используются в Национальных программах вакцинации (например, АКДС, вакцина против гемофильной инфекции, гепатита В).
- С вакцинами в организм человека попадает менее 0,1% ртути от всего количества, которое мы получаем из других источников.
- Опасения по поводу безопасности данного консерванта привели к проведению многочисленных исследований; на протяжении 10 лет экспертами ВОЗ проводились исследования по безопасности с тиомерсалом, в результате которых было доказано отсутствие какого-либо токсического воздействия на организм человека.

- Используется при производстве убитых (инактивированных) вакцин (например, инъекционная полиомиелитная вакцина) и для получения анатоксинов - обезвреженного токсина бактерий (например, АДС).
- На стадии очистки вакцины практически весь формальдегид удаляется.
- Количество формальдегида в вакцинах в сотни раз ниже, чем количество, которое может наносить вред человеку (например, пятикомпонентная вакцина против коклюша, дифтерии, столбняка, полиомиелита и гемофильной инфекции содержит менее 0,02% формальдегида на одну дозу или менее 200 частей на миллион).
Кроме вышеперечисленных консервантов, разрешены для использования два других консерванта для вакцин: 2-феноксиэтанол (используется для инактивированной полиовакцины) и фенол (используется для вакцины против брюшного тифа).

- Используются при производстве некоторых вакцин для предупреждения бактериального заражения среды, где выращиваются возбудители болезни.
- Обычно в вакцинах присутствуют лишь следовые количества антибиотиков. Например, вакцина против кори, краснухи и паротита (КПК) содержит менее 25 микрограмм неомицина на одну дозу.
- Пациенты с аллергией на неомицин должны находиться под наблюдением после вакцинации; это даст возможность немедленно начать лечение любых аллергических реакций.

- Адъюванты используются на протяжении нескольких десятилетий для усиления иммунного ответа на введение вакцины. Чаще всего адъюванты входят в состав убитых (инактивированных) и субъединичных вакцин (например, вакцина против гриппа, вакцина против вируса папилломы человека).
- Наиболее давно и часто используемым адъювантом является соль алюминия - алюминий гидрохлорид (Al(OH)3). Он замедляет выход антигена на месте инъекции и продлевает время контакта вакцины с иммунной системой.
- С целью обеспечения безопасности вакцинации, крайне важно, чтобы вакцины с солями алюминия вводились внутримышечно, а не подкожно. Подкожное введение может привести к развитию абсцесса.
- На сегодняшний день существует несколько сотен различных типов адъювантов, которые используются при производстве вакцин.

Адаптировано с http://www.slideshare.net/addisuga/6-immunization-amha Accessed by May 2016
Вакцинация - одно из величайших достижений медицины в истории человечества.
Рассчитайте персональный календарь прививок Вашего малыша! На нашем сайте это можно сделать легко и быстро, даже если некоторые прививки были выполнены "не вовремя".
Рассчитать мойкалендарь прививок
Источники
- ВОЗ. Основы безопасности вакцин. Электронный модуль обучения.
http://ru.vaccine-safety-training.org/ - http://www.who.int/immunization/newsroom/thiomersal_questions_and_answers/ru
Тиомерсал: вопросы и ответы. Октябрь 2011 г.
Дата последнего посещения 15.10.2015 г. - On-line presentation available on http://www.slideshare.net/addisuga/6-immunization-amha Accessed by May 2016
